Алкохолна ферментация. Реакции на ферментация на въглехидрати
ФЕРМЕНТАЦИЯ- набор от процеси на ензимно преобразуване на въглехидрати, извършвани при анаеробни условия. Б. е вътрешен редокс процес, с помощта на който много организми получават хим. енергия от глюкоза и други вещества в отсъствието на молекулярен кислород. Б. се счита за най-простата форма на биол, механизъм, който осигурява енергия от хранителни вещества.
Ролята на крайния продукт в B. обикновено играе някаква органична молекула, образувана по време на самия процес на B. (алкохол, млечна киселина, маслена киселина и др.). Chem. естеството на тези продукти зависи преди всичко от вида на микроорганизма, който извършва анаеробното превръщане на въглехидратите. Голямо значениеБ. също имат условия за протичане на Б., в зависимост от които един и същ микроорганизъм извършва Б. не само с различна скорост, но и с образуването на различни продукти.
Продуктите, образувани в хода на Б., се използват частично от самите микроорганизми в хода на тяхната жизнена дейност (развитие, растеж, натрупване на обща биомаса). Chem. трансформациите на първоначалния субстрат, възникващи в хода на Б., са придружени от използването на определена част от съдържащия се в него химикал. (безплатна) енергия за задоволяване на нуждите на тялото от енергия и натрупването й под формата на богати на енергия (високоенергийни) съединения, най-важният представител на които е аденозинтрифосфорната киселина (виж). Така Б. е един от видовете енергиен метаболизъм, Характеристика на това е ниският коефициент на използване на свободната енергия, която се съдържа в молекулите на органичното вещество, което е изложено на B. Ниската енергийна ефективност се дължи на факта, че свободният кислород не се използва в процеса на B. .
Началото на интензивното изучаване на Б. е свързано с описанието на дрождените клетки [Kanyar-Latour (VS Cagniard-Latour) във Франция и T. Schwann в Германия, 1836-1838 г.]. Сред учените, които са го изследвали, са Л. Пастьор и 10. Либих. Пастьор, който нарича B. "живот без кислород", вярва, че това може да бъде причинено само от живи дрождени клетки. За разлика от това, Либих разглежда ферментацията на захарта като сложен химичен процес. реакция, която не изисква участието на живи организми. Дългият спор по този въпрос, който има не само чисто научно, но и философско значение, най-накрая беше разрешен в резултат на работата на М. М. Манасейна (1871) и по-специално Е. Бюхнер (1897), който показа способността от безклетъчен сок от дрожди за предизвикване на алкохолна ферментация. Така беше доказано, че B. е ензимен процес, който протича без участието на живи клетки.
По-нататъшни изследвания на природата на B. показват, че цели ензимни системи, комбинирани преди това под често срещано име"зимази" (вж. Ензими). Успоредно с това имаше изясняване на хим. естеството на продуктите, образувани по време на B.
изключителна роля в решаването на тези предизвикателни задачиизиграха изследванията на руски и съветски учени (А. Н. Лебедев, Л. А. Иванов, В. И. Паладий, С. П. Костичев, Я. О. Парнас и др.), както и чуждестранни [Харден (А. Харден), К. Нойберг, О. Майерхоф, Г. Ембден и др.]. По-специално, А. Н. Лебедев предложи нов, по-прост метод за получаване на безклетъчни ензимни препаратиот дрожди чрез автолиза (самосмилане). От основно значение за изясняване на химията на Б. беше откритието на Л. А. Иванов, който показа (1905), че с алкохол Б. не се разлага свободната захарна молекула, а комбинацията от последната с фосфорна киселина (фосфорилирана захар молекула). Последвалите проучвания не само потвърдиха заключенията на Л. А. Иванов, но също така направиха възможно да се гарантира, че реакциите на фосфорилиране в Б. играят ключова роля (виж Гликолиза).
В зависимост от естеството на крайния продукт, образуван по време на процеса, има няколко вида B.
Алкохолна ферментация
Алкохолната ферментация се извършва т.нар. дрождеподобни организми (Monilia, Oidium и др.), както и някои от плесени(напр. брашно).
Алкохолът може да се произвежда и от клетките висши растенияако са в среда с лишен от кислород. При тези условия окислителният метаболизъм на растенията се извършва по пътя, близък до алкохола B. И накрая, в някои тъкани на висши растения (например клетки на точки на растеж или така наречените меристеми), образуването на алкохол е също се наблюдава при условия на пълно снабдяване с кислород. Този вид процеси се наричат аеробна ферментация, ръбове в техния химичен състав. природата също се доближава до алкохол Б.
Алкохолната ферментация се изразява чрез общото уравнение на реакцията: C 6 H 12 O 6 \u003d 2CO 2 + 2C 2 H 5 OH.
От това следва, че при пълната ферментация на 1 мол хексоза, 2 мола въглероден диоксид и 2 мола етилов алкохол. Количеството свободна енергия, реализирано по време на този процес, теоретично трябва да бъде 56 kcal на 1 mol ферментирала хексоза, което е само малка част от енергийния изход, който се получава при нормално аеробно дишане(виж Аероби). В резултат на това да се получи същото количество енергия анаеробни организми(виж Анаероби) трябва да се изразходват за поне 10 пъти голямо количествозахари, отколкото аеробни организми.
Общото уравнение на алкохол Б. не отчита, че в допълнение към етилов алкохол и въглероден диоксид, в хода на Б. се образуват някои други съединения в малки количества. Те включват амилови алкохоли (виж), бутилови алкохоли (виж) и някои други, които заедно образуват т.нар. сивушни масла (виж). Сред продуктите на алкохол Б., ацеталдехид, янтарна киселина и редица други съединения, които придават специфичен аромат и вкус на вино, бира и други алкохолни напитки.
С алкохол Б. се използват захарни молекули с различна степен на сложност. Дрождите ферментират най-лесно глюкозата и фруктозата, много по-лошо е манозата и особено галактозата. Захарозата и малтозата се ферментират само след предварителна хидролиза. Лактозата може да бъде само ферментирала специални видоведрожди, съдържащи ензим, който хидролизира този дизахарид до образуване на глюкоза и галактоза.
При наличието на кислород в околната среда енергийният обмен на дрождите се извършва по пътя на нормалната аеробна трансформация, което прави възможно изразходването на захарта много по-икономично. Захароспестяващият ефект на кислорода е открит за първи път от Л. Пастьор, във връзка с което става известен като ефект на Пастьор.
Първите етапи на трансформации, до-Крим е изложен на глюкоза при алкохол Б., се състои в активиране на захарна молекула. Активирането се осъществява постепенно, чрез поредица от последователни индивидуални реакции. Първата стъпка в отглеждането реактивностглюкозна молекула е образуването на нейния фосфорен естер. Молекулата на аденозин трифосфат (АТФ) става източник на фосфор до-ти, ръбове, давайки тази група, се превръща в аденозин дифосфат (АДФ). Прехвърлянето на фосфатния остатък от АТФ към глюкоза се извършва с участието на ензима хексокиназа (виж).
Този етап е свързан с потреблението на енергия на една макроергична връзка на молекулата на АТФ.
Следващата стъпка е да се изомеризира глюкозо-6-фосфатната молекула и да се превърне във фруктозо-6-фосфат. Процесът се осъществява от ензима глюкозофосфат изомераза [EC 5. 3. 1. 9], който се намира както в дрождите, така и в много други микроорганизми и в тъканите Голям брой различни видоверастения и животни. Активирането на фруктозо-6-фосфат се постига чрез свързване на още един остатък от фосфорна киселина към молекулата и образуване на фруктозо-1,6-дифосфат.
Източникът на фосфат и енергията, необходима за тази реакция, също е молекулата АТФ. Реакцията се катализира от ензима фосфофруктокиназа [K F 2. 7. 1. 11]. Следващата стъпка е образуването на две фосфотриози от молекулата на фруктозо-1,6-дифосфат - дихидроксиацетон фосфат и глицералдехид фосфат (GAF). Ензимът, катализиращ тази реакция, се нарича алдолаза (виж).
Във връзка с особеностите на ензимните системи, участващи в алкохола B., от двете посочени фосфотриози, само GAF участва в по-нататъшни трансформации, което би трябвало да доведе до загуба на половината от първоначалната глюкозна молекула за процеса B. Тази загуба обаче се предотвратява поради наличието в клетката на специфичен ензим - фосфотриоза изомераза, който катализира обратима реакция: дихидроксиацетон фосфат<->глицералдехид фосфат. Това гарантира, че може да се използва цялата захарна молекула.
Окисляването на GAF се катализира от глицералдехид фосфат дехидрогеназа (GAPD) и води до образуването на богато на енергия съединение, 1,3-дифосфоглицерат (1,3 DFG). Общото уравнение на реакцията може да бъде представено по следния начин:
Реакцията протича на няколко етапа: една от SH групите на GAPDH участва в добавянето на NAD + и образуването на комплекс - 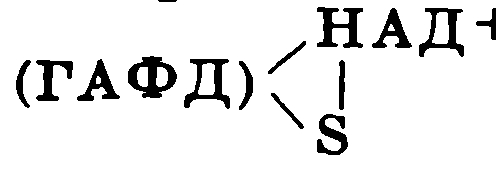 .
.
GAF се добавя към този комплекс, той се окислява с образуването на ацилензим:

След това водородът се прехвърля към NAD+:
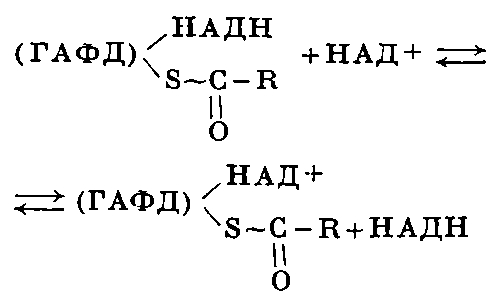
и транспортиране на ацил към неорганичен фосфатен остатък за образуване на 1,3-дифосфоглицерат:
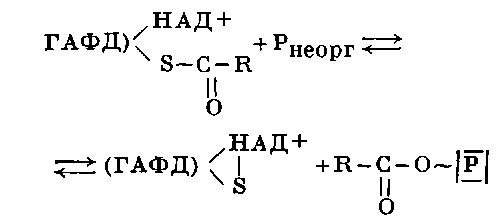
Богатата на енергия връзка на остатъка от фосфорна киселина в молекулата 1.3 DFG позволява образуването на АТФ и 3-фосфоглицеринова киселина:
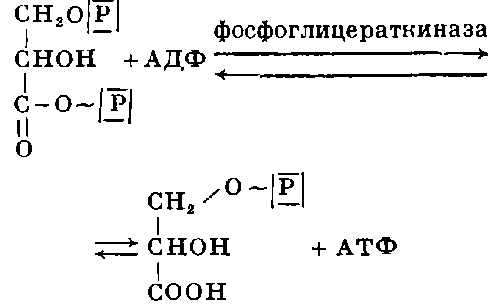
Вътрешномолекулярното движение на фосфатния остатък с участието на фосфоглицеромутаза води до образуването на 2-фосфоглицерол, който след това се превръща във фосфоенолпировинова киселина. По време на дефосфорилирането на фосфоенолпирогроздена киселина и нейното превръщане в пирогроздена киселина (пируват), разцепеният фосфат се прехвърля към ADP. Енергията на двете ATP молекули, образувани на този етап, е чистата печалба от енергия, която клетката придобива в хода на цялата сложна верига от процеси, описани по-горе. Тези процеси са универсални по своята същност и формират основата не само на алкохола, но и на много други видове B. и предимно хомоферментативни млечни B., наречени гликолиза (виж). Много е важно да се отбележи, че изброените реакции водят до образуване на пируват, използван като субстрат биол, окисления (виж Биологично окисление) или дъх.
При анаеробни условия могат да протичат трансформации на пируват различни начини. Така, в случай на алкохол B., CO2 се отцепва от пируват с участието на ензима декарбоксилаза и се образува ацеталдехид:
CH 3 -CO-COOH → CO 2 + CH 3 CHO.
С участието на специфичен ензим (алкохолдехидрогеназа) оцетният алдехид се редуцира до образуване на крайния продукт на алкохол Б. - етилов алкохол. Необходимият за тази реакция водород се получава от редуцирания коензим - никотинамидаденин динуклеотид или NAD-H. Ако редукцията на ацеталдехида се предотврати по някакъв начин (например чрез свързването му с натриев бисулфит), тогава NADH водородът може, с участието на ензима глицерофосфат дехидрогеназа, да реагира с фосфотриози и да доведе до образуването на глицерофосфат, а след това глицерол.
Един от странични продуктиалкохол B. е ацетоин (ацетилметилкарбинол), CH 3 -CO-CHOH-CH 3, който се образува при взаимодействието на две молекули пирогроздена киселина или пирогроздена киселина с оцетен алдехид:
CH 3 COCOOH + CH3COH → CH 3 COCHOH-CH 3 + CO 2.
Образува се по време на т.нар. реакция на карболигас, катализирана от ензими, изолирани от клетки на дрожди и от висши растения. Ацетоинът се образува и в други видове B. Ацетоинът е лесно разтворим във вода, алкохол и етер. Трябва да се спомене още един междинни продуктиразграждането на въглехидратите в Б., което също е производно на пирувинова киселина. Това е метилглиоксал (CH 3 COCHO), който по свой начин химическа природапредставлява пируват алдехид. При нагряване с вода или при алкализиране водни разтвориметилглиоксалът се превръща в млечна киселина. Може да се образува и ензимно – под действието на специфичен ензим метилглиоксилаза. Тези съединения се образуват в много малки количества.
млечнокисела ферментация
Генетично свързан с алкохола Б. млечнокисела ферментация, която има много важност. В този случай пирогроздената киселина не се декарбоксилира, както при алкохолната В., а се редуцира директно с участието на специфична лактатдехидрогеназа за сметка на NADH водород.
Има две групи млечнокисели бактерии. Първият от тях включва хомоферментативни бактерии, които образуват само млечна киселина. Млечнокисели бактерии от втората група (хетероферментативни бактерии) образуват, в допълнение към млечната, също оцетна киселина, както и етилов алкохол (често в много значителни количества), въглероден двуокис, мравчена киселина и някои други продукти. Съотношението между тези продукти зависи от много условия (температура, pH на средата и др.). Често това се дължи на съвместната дейност на млечнокисели бактерии с дрожди. Този вид съвместна „закваска“ често се създава изкуствено и се използва широко в пекарството - при готвене ръжен хляб, в производство хлебен кваси редица млечнокисели продукти (сирене, кефир, изварено мляко, кумис и др.). Страхотно приложениенамира млечна киселина Б. в производството на млечна киселина, която се използва в редица отрасли на хранителната, текстилната и кожарската промишленост.
Особено ефективна млечна киселина Б. се извършва от термофилни микроби от типа Thermobacterium cereale (наричан по-рано Lactobacillus delbrukii). Млечната киселина се образува и като един от продуктите на превръщането на въглехидратите в мускулна тъканживотни по време на гликолиза.
Маслена ферментация
Маслената ферментация се извършва в повечето случаи от облигатни анаероби, т.е. организми, които могат да съществуват само в среда без кислород.
В хода на маслена Б. се образува не само маслена киселина, но в някои случаи много големи количества етилов алкохол, млечна и оцетна киселина, както и газообразен водород и въглероден диоксид. С помощта на маслена Б. се извършва разлагане органична материяв условия на липса или пълна липса на кислород (блата, влажни зони). От голямо индустриално значение е масленият Б. на пектин, който се получава по време на заключването на ленени и конопени стъбла и производството на влакна. В същото време трябва да се предотврати активността на бактериите, които извършват този тип Б., когато се приготвят различни видове хранителни продуктиза да се избегне влошаване на вкуса и разваляне на последния (например гранясване масло, силози и др.).
Алкохолни, млечни и маслени Б. са основните видове Б.; останалите многобройни видове Б. са или различни комбинации от тях, или се извършват на базата на определени продукти, които възникват в хода на основния тип Б. Така че, в резултат оцетна ферментацияетилов алкохол се окислява с участието на атмосферен кислород. Този тип B. се извършва от специфични оцетнокисели бактерии. Общото уравнение на оцетната киселина B.:
CH 3 CH 2 OH + O 2 \u003d CH 3 COOH + H 2 O.
След като запасите от алкохол се изчерпят, бактериите окисляват образуваната от него оцетна киселина до въглероден диоксид и вода.
Б., извършено с участието на О 2, включва глюконатна ферментация- образуване на глюконова киселина от глюкоза:
C 6 H 12 O 6 + H 2 O + O 2 → CH 2 OH (CHOH) 4 COOH + H 2 O 2.
Причинява се от определени бактерии и гъбички. Глюконовата киселина е ценно съединение, широко използвано в медицината, фармацевтиката и индустрията (вижте Глюконова киселина).
Ферментация с лимонена киселинаизвършвани от определени представители на плесени; определени щамове на Aspergillus niger са особено ефективни. Първоначалният продукт е пирувинова к-та, трансформацията на рояк протича едновременно в две посоки. Част от него се окислява до оцетна киселина, а другата чрез добавяне на въглероден диоксид образува оксалооцетна киселина. Когато оцетната и оксалооцетната киселина се кондензират, се образува лимонена киселина. В допълнение към лимонената киселина, цитрат Б. произвежда бутилов алкохол, ацетон, както и етилов алкохол, въглероден диоксид и водород.
Бутанол-ацетонова ферментацияизвършвам анаеробни бактерии Clostridium acetobutylicum. Основните продукти, образувани по време на този тип B., са n-бутилов алкохол, ацетон, етилов алкохол, въглероден диоксид и водород. Ацетооцетната до - тази (CH 3 COCH 2 COOH) и ацетонът (CH 3 COCH 3), образуван при нейното декарбоксилиране, както и β-хидроксимаслената до -, които съставляват групата на т.нар. ацетонови тела (вж. Кетонни тела), които се натрупват в кръвта и урината на животните по време на различни патологични състоянияи заболявания (диабет, глад). При нормални условия тези съединения се окисляват, за да образуват въглероден диоксид и вода, които са безвредни за тялото.
Висока икономическа ефективност, чистота, получена с B. ценни продуктилежат в основата все повече и повече широко използванеБ. в различни сектори на националната икономика.
Библиография:Кретович В.Л. Основи на биохимията на растенията, М., 1971; Малер Г. и Кордес Ю. Основи биологична химия, пер. от англ., М., 1970; Рубин Б. А. Курс по физиология на растенията, М., 1971; Рекер Е. Биоенергийни механизми, прев. от англ., М., 1967. Библиография; Шапошников В. Н. Техническа микробиология, М., 1948; H as s i d W. Z. Трансформация на захари в растенията, Ann. Rev. растителна физиология, v. 18, стр. 253, 1967, библиогр.
Ферментацията е сложен процес на разграждане на въглехидрати под въздействието на ензими, секретирани от различни микроорганизми, в повечето случаи придружен от отделяне на газообразни продукти (CO 2, H 2 и др.) и в крайна сметка водещ до образуването на вещества като етилов алкохол , млечна киселина и др. В зависимост от вида на микроорганизма и крайни продуктиИма няколко вида ферментация:
Алкохолна ферментация: C 6 H 12 O 6 → 2CH 3 ─ CH 2 ─ OH + 2CO 2
Глюкоза Етанол
Млечнокисела ферментация: C 6 H 12 O 6 → 2CH 3 ─ CHOH ─ COOH
Глюкоза Млечна киселина
Оцетна ферментация: C 6 H 12 O 6 + 2O 2 → 2CH 3 ─ COOH + 2CO 2 + 2H 2 O
Глюкоза Оцетна киселина
Ферментация на пропионова киселина: C 6 H 12 O 6 → 2CH 3 ─ CH 2 ─ COOH + O 2
Глюкоза пропионова киселина
Маслена ферментация: C 6 H 12 O 6 →CH 3 ─CH 2 ─CH 2 ─ COOH + 2CO 2 + 2H 2
Глюкоза Маслена киселина
Ферментация на лимонена киселина: 2C 6 H 12 O 6 + 3O 2 → CH 2 ─ COOH
Глюкоза │
2HO ─ C ─ COOH + 4H 2 O
Метанова ферментация: C 6 H 12 O 6 → 3CH 4 + 3CO 2
Глюкоза метан
Алкохолната ферментация се използва в промишлеността за получаване на етилов алкохол, млечнокиселата ферментация - в Хранително-вкусовата промишленостза получаване на различни млечнокисели продукти и в животновъдството по време на силажиране на фураж. Оцетна киселина, пропионова киселина, маслена киселина, млечнокисела ферментациясе срещат в панкреаса на преживните животни. Ферментацията на метан причинява тимпания (подуване) при многостомашни животни. Само хексозите се подлагат на алкохолна ферментация, за разлика от други монозахариди, като пентозите. Това се използва за разграничаване на хексози от пентози. Малтозата и захарозата лесно се ферментират от дрожди, но лактозата не. Дрождите имат ензимите малтаза и сукраза, но не и ензима лактаза. Лактозата, под въздействието на бактерии, които я разграждат, може да доведе до алкохолна, млечна и маслена ферментация.
Задача: Направете изводи по темата „Въглехидрати:
Урок 5 - Структурата на протеините
Цел на урока: Изучаване на структурата на протеините
Реактиви: Протеинови разтвори: яйце и желатин, 1% разтвор на меден сулфат, 10% и 20% разтвори на натриев хидроксид, 0,2% разтвор на нинхидрин, 0,5% разтвор на оловен ацетат.
1. Общи качествени реакции към протеини: биурет - към пептидна връзка, нинхидрин - към α-аминогрупи на аминокиселини
Принципът на метода.Биуретовата реакция е качествена реакция на пептидна връзка. Реакцията се основава на образуването на вътрешнокомплексно съединение от медни йони с две пептидни връзки, действащи като полидентатни лиганди. В алкална среда протеиновият разтвор, когато се добави разреден разтвор на меден сулфат, става розово-виолетов:
H 2 N-CH-CO-NH-CH-CO-NH-CH-CO-NH-CH-C \u003d O + 2NaOH + Cu (OH) 2
R1R2R3R4OH
NH-CH-C=N-CH-C-N-CH-C-... 2-
R 4 O R 6 O 2Na +
NH-CH-C-N-CH-C=N-CH-C-...
Реакцията се нарича биурет, тъй като е характерна и за биурета, състоящ се от 2 молекули урея (NH 2 -CO-NH-CO-NH 2).
Напредък. биуретова реакция.В отделни епруветки изсипете 1 ml разтвори на изследваните протеини: яйчен белтък, желатин, кръвен серум. След това добавете 1 ml 10 % р-ра NaOH и 2 капки 5% р-ра CuS0 4 . След разбъркване при наличие на пептидна връзка в изследваните разтвори се появява виолетов цвят.
Нинхидринова реакция. Към 2 ml от изследваните протеинови разтвори се добавят 10-12 капки нинхидрин, загряват се, наблюдава се синьо-виолетово оцветяване - продукт на взаимодействието на аминогрупата на аминокиселините с нинхидрин.
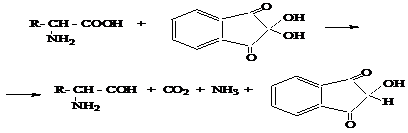
намален нинхидрин

Синьо-виолетов кондензат
Подобни статии
-
Когато съпругът е против дете, как да забременеете без негово знание?
Понякога можете да забременеете по небрежност. За да не се случи това, е важно да знаете как можете да заченете дете случайно и какви средства можете да използвате, за да избегнете нежелана бременност. Също така в тази статия можете да намерите информация за...
-
Какви камъни и амулети са подходящи за Телец според хороскопа и датата на раждане Талисман на слон за Телец
Април-май Телците (21 април - 20 май) са премерени, не са суетливи и колосално продуктивни! Тяхната завидна упоритост може да доведе другите до дръжката, но те знаят точно какво правят и защо имат нужда от това. Сред положителните...
-
Ограничения за достъп до данни в роли 1c
Всички настройки на потребителските права, които ще направим в рамките на тази статия, се намират в раздел 1C 8.3 "Администриране" - "Настройки на потребител и права". Този алгоритъм е подобен в повечето конфигурации на ...
-
1c стартира тънък клиент вместо дебел
Платформи: 1C: Enterprise 8.3, 1C: Enterprise 8.2, 1C: Enterprise 8.1 Конфигурации: Всички конфигурации2012-11-16 21362 Те се стартират чрез указване на специални ...
-
Доказателства за известни начини за кражба на ток Как да разберете кой краде ток
Повишаването на енергийните тарифи е една от поразителните характеристики на задълбочаващата се икономическа криза. В този контекст кражбата на електроенергия и проблемите, свързани с разкриването й, са от първостепенно значение.Начини за разкриване на кражба ...
-
Характеристики на монтаж на контакти и превключватели на различни повърхности
Поздрави на всички читатели на нашия блог Днес, скъпи читатели, искам да подчертая темата как да инсталирам гнезда. Тази процедура е много често търсена при подмяна на стар контакт с нов в случай на повреда, когато ...
